Η FDA “ΕΝΕΚΡΙΝΕ” ΤΟ COMIRNATY PFIZER-BIONTECH(ΕΝΑ ΜΕΛΟΝΤΙΚΟ ΕΜΒΟΛΙΟ)ΤΟ "ΕΜΒΟΛΙΟ" ΤΕΛΕΙ ΑΚΟΜΑ ΥΠΟ ΕΓΚΡΙΣΗ ΕΚΤΑΚΤΗΣ ΑΝΑΓΚΗΣ (EUA),
Για όσους σας λένε ότι η ένεση κατά της Covid-19 είναι εξουσιοδοτημένη, εγκεκριμένη ή αδειοδοτημένη, απαντήστε τους με γεγονότα και δεδομένα, ειδικά εκείνους που θεωρούν ότι η ένεση C19 είναι καλή ιδέα για τα παιδιά.
Πριν απο μερικές μέρες (23.08.2021), η FDA “ενέκρινε” το Comirnaty (Pfizer-BioNTech) αν και αδυνατούμε να καταλάβουμε τί ακριβώς είναι αυτή η έγκριση μιας και το “εμβόλιο”, σύμφωνα με την ανακοίνωση, παραμένει υπο άδεια χρήσης έκτακτης ανάγκης.
Οι ενέσεις βρίσκονται ακόμη στο στάδιο 3 των κλινικών δοκιμών που δεν θα ολοκληρωθούν πριν από τις αρχές του 2023.
Επί του παρόντος, η έγκριση έκτακτης ανάγκης (EUA), η άδεια κυκλοφορίας υπό όρους (Conditional Marketing Authorisation-CMA) κ.λπ., όλοι αυτοί οι όροι σημαίνουν ότι χρησιμοποιούνται μόνο λόγω “έκτακτης ανάγκης”.
Κλινικές δοκιμές AstraZeneca
Κλινικές δοκιμές BioNTech/Pfizer
Το Conditional Marketing Authorisation του Vaxzevria (AstraZeneca).
To EMERGENCY USE AUTHORIZATION (EUA) του
Όσο για τις παρενέργειες, τις γνωρίζουμε πλέον όλοι και όμως, το Ελληνικό κράτος και ο ΕΟΦ αρνούνται να λάβουν τα δεδομένα στα σοβαρά.

Το κοινό θα πρέπει να αρχίσει να χρησιμοποιεί φάρμακα ή εμβόλια που βρίσκονται στο στάδιο 4 των κλινικών δοκιμών. Η Pfizer στην ιστοσελίδα της αναφέρει τα εξής:
Η κλινική δοκιμή είναι μια ερευνητική μελέτη που διερευνά κατά πόσον μια ιατρική θεραπεία ή συσκευή είναι ασφαλής και αποτελεσματική για τον άνθρωπο. Διαδραματίζει κρίσιμο ρόλο στη διαδικασία προώθησης νέων θεραπειών στους ασθενείς.
Κατά μέσο όρο χρειάζονται 12 χρόνια για να αναπτυχθεί και να εγκριθεί η χρήση μιας πιθανής νέας θεραπείας σε ασθενείς, αν και ο χρόνος ποικίλλει σημαντικά ανάλογα με την πολυπλοκότητα και την επιτυχία της νέας θεραπείας.
Ενώ η ανάπτυξη ενός εμβολίου για την καταπολέμηση του COVID-19 επιτεύχθηκε σε λιγότερο από ένα χρόνο, βασίστηκε σε δύο δεκαετίες προηγούμενης έρευνας και ανάπτυξης, ομοίως η πρώτη γονιδιακή θεραπεία χρειάστηκε περισσότερα από 20 χρόνια για να φτάσει στους ασθενείς.
Οι δοκιμές σε ζώα για εμβόλια κατά της Covid απέτυχαν πάντοτε επειδή τα ζώα αρρώστησαν ή πέθαναν.
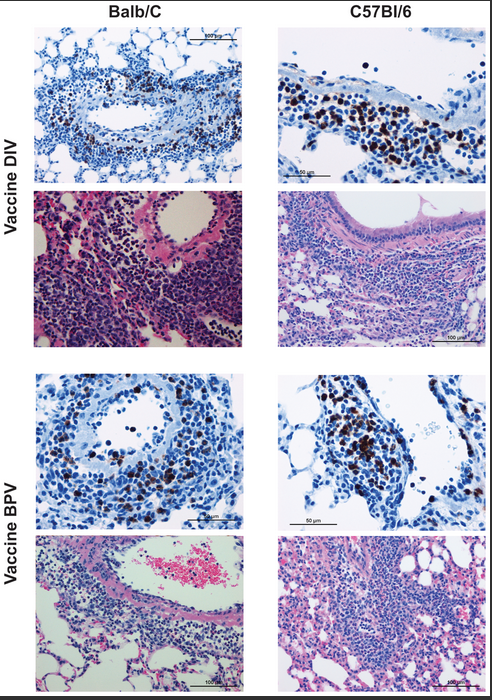
Η μελέτη που πραγματοποιήθηκε το 2012 αξιολόγησε ένα αδρανοποιημένο εμβολίου ολόκληρου του ιού σε κουνάβια και πρωτεύοντα θηλαστικά και ενός εμβολίου που μοιάζει με σωματίδιο ιού σε ποντίκια.
Τα εμβόλια επέφεραν προστασία έναντι της λοίμωξης, αλλά τα προσβεβλημένα ζώα παρουσίασαν ανοσοπαθολογικού τύπου πνευμονική νόσο.
Η μελέτη συμπεραίνει οτι όλα αυτά τα εμβόλια SARS-CoV προκάλεσαν αντισώματα και προστασία από τη μόλυνση με SARS-CoV. Ωστόσο, η δοκιμή σε ποντίκια στα οποία χορηγήθηκε οποιοδήποτε από τα εμβόλια οδήγησε σε εμφάνιση ανοσοπαθολογίας τύπου Th2, γεγονός που υποδηλώνει ότι προκλήθηκε υπερευαισθησία στα συστατικά του SARS-CoV. Ενδείκνυται προσοχή στην εφαρμογή εμβολίου SARS-CoV σε ανθρώπους
.

Η μελέτη αυτή του 2007 τονίζει οτι , παρόλο που τα εμβόλια VRP-S παρείχαν πλήρη βραχυπρόθεσμη προστασία έναντι ετερόλογης πρόκλησης icGD03-S σε νεαρά ποντίκια, μόνο περιορισμένη προστασία παρατηρήθηκε σε εμβολιασμένα γερασμένα ζώα.
Τα εμβόλια VRP-N όχι μόνο δεν κατάφεραν να προστατεύσουν από την ομόλογη ή ετερόλογη πρόκληση, αλλά οδήγησαν σε ενισχυμένη ανοσοπαθολογία με ηωσινόφιλες διηθήσεις στους πνεύμονες των ποντικών που προσβλήθηκαν από SARS-CoV.
Η επαγόμενη από το VRP-N παθολογία παρουσιάστηκε την ημέρα 4, κορυφώθηκε γύρω στην ημέρα 7 και παρέμεινε έως την ημέρα 14 και πιθανώς διαμεσολαβείται από κυτταρικές ανοσολογικές αποκρίσεις.
Η εκτεταμένη αυτή μελέτη πραγματοποιήθηκε το 2008 σε ποντίκια εργαστηρίου. Η μελέτη καταλήγει τονίζοντας “ότι η ανοσοποίηση ποντικών BALB/c με την πρωτεΐνη N του SARS-CoV προκαλεί σοβαρή πνευμονική φλεγμονή κατά την επακόλουθη μόλυνση από τον SARS-CoV, πιθανώς μέσω της ανισορροπίας που δημιουργείται μεταξύ της ενεργοποίησης και της καταστολής των Τ-κυττάρων, καθώς και μέσω της μαζικής παραγωγής προφλεγμονωδών κυτταροκινών. “
Οι αρχικές μελέτες ήταν σύντομες και λανθασμένες
Το παρασκεύασμα της BioNTech/Pfizer
Το εμβόλιο COVID-19 της Pfizer (BNT162b2), που τώρα ονομάζεται Comirnaty, είναι η πρώτη εμπορική παραγωγή εμβολίου mRNA – ένα εντελώς νέο είδος βιοτεχνολογίας. Αυτό δεν λειτουργεί με τον ίδιο τρόπο όπως τα συμβατικά εμβόλια.
Εμβόλια mRNA έχουν επιχειρηθεί προηγουμένως για άλλους κορονοϊούς, π.χ. MERS και SARS- ωστόσο, αυτά ήταν ανεπιτυχή λόγω υψηλών επιπέδων παρενεργειών στις μελέτες σε ζώα.
Το εμβόλιο χρησιμοποιεί ένα σκέλος συνθετικού mRNA. Το mRNA είναι ασταθές και γι’ αυτό συσκευάζεται μέσα σε νανοσωματίδια λιπιδίων , τα οποία είναι μικροσκοπικά σωματίδια καλυμμένα με PEG (πολυαιθυλενογλυκόλη – μια χημική ουσία με βάση το πετρέλαιο). Τα νανοσωματίδια προστατεύουν το mRNA και του επιτρέπουν να εισέλθει στα κύτταρα του σώματος μετά τον εμβολιασμό.
Όταν το mRNA εισέρχεται σε ένα κύτταρο, χρησιμοποιεί τον κυτταρικό μηχανισμό, παρέχοντας οδηγίες για να το κύτταρο να παράγει πρωτεΐνες αιχμής του κοροναϊού, οι οποίες απελευθερώνονται στο κυκλοφορία του αίματος.
Το ανοσοποιητικό σύστημα αναγνωρίζει αυτές τις πρωτεΐνες ως ξένες και παράγει αντισώματα εναντίον τους, τα οποία πιστεύεται ότι παρέχουν ανοσία κατά μιας μελλοντικής λοίμωξης από τον SARS-CoV-2.
Απαιτούνται δύο δόσεις.
Η διάρκεια της ανοσίας είναι άγνωστη, λόγω περιορισμένων δεδομένων, καθώς οι μελέτες έχουν δεν έχουν ακόμη ολοκληρωθεί. Η ανοσία πιστεύεται ότι διαρκεί τουλάχιστον 2 μήνες.
Δεν έχουν δημοσιευθεί μελέτες ασφάλειας σε ζώα για το εμβόλιο αυτό. Το εμβόλιο δοκιμάστηκε σε ποντίκια και μακάκους πιθήκους για να διαπιστωθεί μόνο η αποτελεσματικότητα (όχι η ασφάλεια).
Δοκιμές εμβολίων mRNA για άλλους κορονοϊούς οδήγησαν σε σοβαρές παρενέργειες, λόγω ενός φαινομένου που ονομάζεται Εξαρτώμενη από τα αντισώματα ενισχυμένη ανοσία (ADE-Antibody Dependent Enhanced Immunity).
Αυτό συμβαίνει όταν τα αντισώματα που προκαλούνται από το εμβόλιο προκαλούν παραδόξως σοβαρότερη ασθένεια με την επακόλουθη έκθεση στον ιό. Πολλά ζώα που συμμετείχαν πέθαναν ή έγιναν πολύ άρρωστα και οι δοκιμές σε ανθρώπους δεν συνεχίστηκαν.
Η Pfizer ανέφερε (βλ. παρουσίαση του CDC) μια σύντομη μελέτη ασφάλειας σε αρουραίους Wistar χωρίς να εντοπιστούν συστηματικά συμβάντα, ωστόσο η μελέτη αυτή δεν είναι διαθέσιμη στο κοινό.
Μελέτες αποτελεσματικότητας: τόσο τα ποντίκια όσο και οι μακάκοι ανέπτυξαν αντισώματα κατά του SARS-CoV-2 μετά την ανοσοποίηση. Μετά τον εμβολιασμό, όταν εκτέθηκαν σκόπιμα στον SARS-CoV-2, όλοι οι πίθηκοι είχαν ενδείξεις μόλυνσης με SARS-CoV-2 στη μύτη και τους αεραγωγούς τους.
Κανένας από τους πιθήκους, είτε στην ομάδα εμβολιασμού είτε στην ομάδα εικονικού φαρμάκου(placebo), δεν εμφάνισε συμπτώματα. Τα ζώα που έλαβαν το εμβόλιο είχαν ενδείξεις SARS-CoV-2 στη μύτη τους για 1 ημέρα, ενώ εκείνα που έλαβαν το εικονικό φάρμακο είχαν SARS-CoV-2 σε ρινικά επιχρίσματα τις ημέρες 1, 3 και 6 μετά την έκθεση.
Καθώς κανένα ζώο σε καμία από τις δύο ομάδες δεν εμφάνισε συμπτώματα, δεν μπορούμε να συμπεράνουμε αν το εμβόλιο θα μείωνε τα συμπτώματα στους ανθρώπους. Δεν πραγματοποιήθηκε αξιολόγηση της μετάδοσης.
Δοκιμές φάσης 1 & 2:
204 άτομα έλαβαν 2 δόσεις του εμβολίου BNT162b2 (άλλοι έλαβαν εικονικό φάρμακο ή ένα πιθανό εναλλακτικό εμβόλιο). Οι συμμετέχοντες παρείχαν ημερήσιο ημερολόγιο, για έναν κατάλογο παρενεργειών, επί 7 ημέρες μετά τη λήψη του εμβολίου.
Ορισμένοι ανέφεραν πονοκεφάλους, μυϊκούς και αρθρικούς πόνους που τους εξουθένωναν και τους εμπόδιζαν να εκτελούν ακόμη και βασικές καθημερινές εργασίες. Η αποτελεσματικότητα της φάσης 2 θα μετρηθεί για 24 μήνες, ενώ η ασφάλεια θα παρακολουθείται για 6 μήνες.
Ο αριθμός των λεμφοκυττάρων παρακολουθήθηκε στα 24 άτομα που έλαβαν το εμβόλιο στη Φάση 1, κατά τα άλλα δεν έγιναν αιματολογικές εξετάσεις για να εκτιμηθεί η πιθανή επίπτωση στα εσωτερικά όργανα ή άλλες πτυχές της υγείας.
Φάση 3:
43.538 άτομα είχαν εγγραφεί στη δοκιμή Φάσης 3 μέχρι τις αρχές Δεκεμβρίου 2020. Η μελέτη δεν θα ολοκληρωθεί πριν από τον Ιανουάριο του 2023- τα άτομα που λαμβάνουν το εμβόλιο θα πρέπει να γνωρίζουν ότι είναι ακόμη ουσιαστικά πειραματικό.
Αποτελεσματικότητα:
Η Pfizer δημοσίευσε ένα δελτίο τύπου στο οποίο αναφέρεται ότι το εμβόλιο είναι αποτελεσματικό κατά 95%. Αυτός ο υπολογισμός της αποτελεσματικότητας βασίζεται μόνο σε 181 από τους 43.548 συμμετέχοντες.
Από τους 43.548 συμμετέχοντες στη δοκιμή, μόνο 181 άτομα είχαν επιβεβαιωμένες περιπτώσεις συμπτωματικής λοίμωξης SARS-CoV-2 (COVID-19) – 1 ή περισσότερα συμπτώματα συν θετικό αποτέλεσμα PCR τουλάχιστον 7 ημέρες μετά τη δεύτερη δόση του εμβολίου.
Από τα 181 “κρούσματα”, το 95% ήταν στην ομάδα του εικονικού φαρμάκου και το 5% στην ομάδα του εμβολίου. Αρκετοί άλλοι συμμετέχοντες εμφάνισαν COVID-19, αλλά αποκλείστηκαν από την ανάλυση λόγω του χρόνου εμφάνισης των συμπτωμάτων τους.
Περισσότερες πληροφορίες θα βρείτε στο παρακάτω PDF.
Το παρασκεύασμα της AstraZeneca
Αυτό το εμβόλιο χρησιμοποιεί έναν αδενοϊό χιμπατζή ως φορέα για να μεταφέρει ένα γονίδιο του ιού SARS-CoV-2 στα κύτταρα του σώματος του λήπτη. Το γονίδιο του ιού SARS-CoV-2 (συνθετικό DNA) που κωδικοποιεί την πρωτεΐνη αιχμής του ιού εισάγεται στον αδενοϊό.
Μετά την έγχυση του εμβολίου, ο αδενοϊός εισβάλλει στα κύτταρα του λήπτη και το γονίδιο του ιού εκφράζεται από τον μηχανισμό του κυττάρου-ξενιστή, ο οποίος αρχίζει να παράγει πρωτεΐνες αιχμής. Αυτές οι πρωτεΐνες εισέρχονται στην κυκλοφορία του αίματος και ο οργανισμός ξεκινά ανοσολογική απόκριση, δημιουργώντας αντισώματα.
Απαιτούμενες δόσεις: Δύο ξεχωριστές δόσεις των 0,5 ml η καθεμία. Η δεύτερη δόση πρέπει να χορηγείται μεταξύ 4 και 12 εβδομάδων μετά την πρώτη δόση.
Δεν υπάρχουν ακόμη πληροφορίες σχετικά με το πόσο καιρό είναι πιθανό να διαρκέσει η ανοσία του εμβολίου, καθώς υπάρχουν διαθέσιμα στοιχεία μόνο μερικών μηνών.
Το εμβόλιο δεν πιστεύεται ότι αποτρέπει τη μετάδοση του ιού, πράγμα που σημαίνει ότι η κοινωνική αποστασιοποίηση θα χρειαστεί πιθανότατα και μετά τον εμβολιασμό.
Είναι άγνωστο πώς θα αντιδράσει στο εμβόλιο κάποιος που έχει ήδη “περάσει” την COVID-19, καθώς οποιοσδήποτε με προηγούμενη έκθεση αποκλείστηκε από τη δοκιμή.
Δεν έχει αποκλειστεί εντελώς το ενδεχόμενο παθογόνου εκκίνησης/εξαρτώμενης από τα αντισώματα ενίσχυσης.
“Καμία από τις δοκιμές που βρίσκονται σε εξέλιξη δεν έχει σχεδιαστεί για να ανιχνεύσει μείωση σε οποιαδήποτε σοβαρή έκβαση, όπως νοσηλείες, χρήση εντατικής θεραπείας ή θανάτους.” δήλωσε ο Peter Doshi, British Medical Journal
Δοκιμές 1ης φάσης: Μια δοκιμή με 1.077 υγιείς ενήλικες ηλικίας 18-55 ετών, 91% Καυκάσιοι, ξεκίνησε στο Ηνωμένο Βασίλειο τον Απρίλιο του 2020. Στην ομάδα του εικονικού φαρμάκου χορηγήθηκε το εμβόλιο κατά της μηνιγγίτιδας (MenACWY) (όχι αδρανές εικονικό αλατούχο φάρμακο). Άτομα με γνωστές υποκείμενες παθήσεις αποκλείστηκαν από τη δοκιμή αυτή.
Δοκιμές φάσης 2/3: Σε μια μονότυπη, τυχαιοποιημένη, ελεγχόμενη δοκιμή, υγιείς ενήλικες > 18 ετών συμμετείχαν σε δύο κλινικές ερευνητικές δοκιμές του Ηνωμένου Βασιλείου. Μετά από δύο δόσεις εμβολίου, αναφέρθηκαν τα ακόλουθα:
Τοπικές ανεπιθύμητες αντιδράσεις (πόνος, ερυθρότητα, οίδημα στο σημείο της ένεσης) αναφέρθηκαν σε 43/49 (88%) συμμετέχοντες στην ομάδα 18-55 ετών, 22/30 (73%) στην ομάδα 56-69 ετών και 30/49 (61%) στην ομάδα 70+ ετών.
Συστηματικές αντιδράσεις (πυρετός, ρίγη, κόπωση, μυϊκός πόνος κ.λπ.) αναφέρθηκαν σε 42 (86%) συμμετέχοντες στην ομάδα 18-55 ετών, 23 (77%) στην ομάδα 56-69 ετών και 32 (65%) στην ομάδα 70+ ετών.
Περισσότερες πληροφορίες θα βρείτε στο ακόλουθο PDF
Ποια είναι τα τελευταία επιστημονικά στοιχεία σχετικά με την αποτελεσματικότητα/αποδοτικότητα αυτών των εμβολίων;
Η απόλυτη μείωση του κινδύνου, δηλαδή ο πραγματικός αντίκτυπος που είχε η ίδια η ένεση στη μείωση των πιθανοτήτων σας να νοσήσετε από την Covid-19, είναι μόλις 0,84% για το Pfizer και 1,28% για το AZ. (Μελέτη)
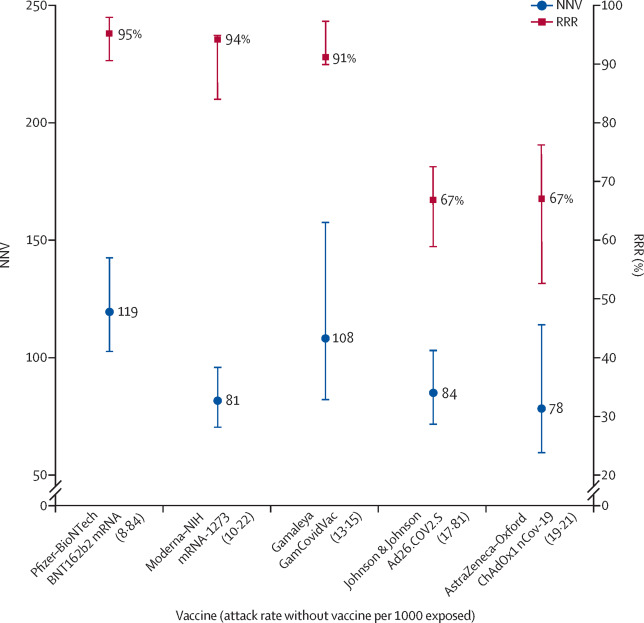
Εάν οι ενέσεις δεν λειτουργούν στις “μεταλλάξεις” (δεδομένου ότι οι άνθρωποι εξακολουθούν να αρρωσταίνουν και να πεθαίνουν και μάλιστα σε αυξανόμενους αριθμούς) , γιατί συνεχίζουν να κάνουν ενέσεις στους ανθρώπους με τις ίδιες πειραματικές ενέσεις που έχει αποδειχθεί ότι δεν λειτουργούν;




Δεν υπάρχουν σχόλια:
Δημοσίευση σχολίου